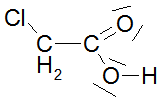|
||
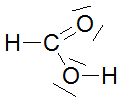
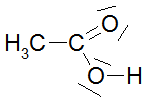
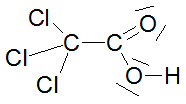
Säurestärke einiger Carbonsäuren (I) |
||
|
Problemstellung:
Welcher
Zusammenhang existiert zwischen Molekülstruktur und Säurestärke (Acidität)?
Dazu werden die in der Tabelle angegebenen Carbonsäuren auf ihre Acidität hin untersucht. Als „Indikator" für diese Eigenschaft wird der pH-Wert und die Heftigkeit der Reaktion mit metallischem Magnesium genommen.Es werden folgende Untersuchungen durchgeführt: 1. Messe zuerst mit dem pH-Messgerät den pH-Wert der Lösung und trage ihn in die Tabelle ein. Die Lösungen haben alle die gleiche Konzentration von 1 mol/l. 2. 25 ml der Lösung werden in ein großes Reagenzglas. mit seitlichem Einsatz eingefüllt, der Kolbenprober dazu angeschlossen und 0,5 g Magnesiumspäne dazugegeben. Nach dem Zuschütten der Mg-Späne muss sofort das Rggl. geschlossen werden. |
||
Es soll die Heftigkeit der Reaktion (sehr stark, stark, mittel, schwach, sehr schwach) beobachtet und die Zeit gemessen werden, bis sich 50 ml Gas entwickelt haben. |
||