Kinetik der alkalischen Esterhydrolyse1. Voraussetzungen |
||||||||
|
Ein Ester reagiert mit Wasser in folgender Gleichgewichtsreaktion: Ester + Wasser <=========>Sõure + Alkohol Die
Esterverbindung ist elektrisch nicht leitend.
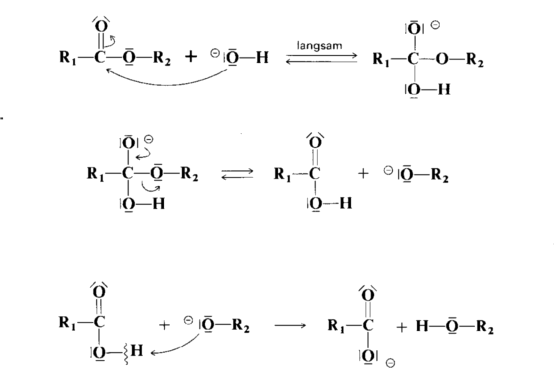
Wird dem Ester Natronlauge zugesetzt, verlõuft folgende
alkalische Hydrolyse-Reaktion
(alkalische Verseifung): |
||||||||
 |
||||||||
| Die
Reaktion verlõuft in
drei Schritten:
1.Nucleophiler Angriff des Hydroxid-Ions unter Bildung eines Additionsprodukts 2. Abspaltung des Alkoholat-Ions und Bildung der Carbonsõure 3. Protonen³bergang vom Carbonsõure-Molek³l auf das Alkoholat-Ion |
||||||||
| 2. Einsatz der Konduktometrischen Methode | ||||||||
| 3. Theorie des Messverfahrens | ||||||||
| Zum Ladungstransport tragen
bei der Reaktion die Natrium-Ionen Na+, die
Hydroxid-Ionen OH
¢ und die Acetationen Ac ¢ bei. Deren
molare Ionenleitfõhigkeit bei unendlicher Verd³nnung besitzen bei 25 ░C
die Werte: OH¢: 199,2 S * cm2/mol, Ac ¢:
40,9 S * cm2/mol und Na+: 50,1 S * cm2/mol
Welche Beziehung besteht nun zwischen der Abnahme der Stromstõrke und der ─nderung der OH¢-Konzentration? Nach einem Drei-Phasen-Modell k÷nnen folgende
Abschnitte der Reaktion unterschieden werden: |
||||||||
|
a). Beginn der Reaktion
Zu Beginn der Reaktion (t = 0) liegen nur die Na+ - und OH¢-Ionen vor. Die Stromstõrke hat daher gemõ▀ der allgemeinen Beziehung [4] I = a * ∑ (m(x) * c(x)) den Wert: I0 = ∑ I (x) = I(Na+) + I(OH¢) [5] Die Stromstõrke ist dabei proportional der Ladung und der Schnelligkeit, mit der die Ladung transportiert wird. Die Gr÷▀e der Ladung und die Geschwindigkeit des Transports werden ausgedr³ckt im Faktor m(x) . Die Anzahl der Ladungstrõger, also die Konzentration, spielt ebenfalls eine Rolle. Daraus ergibt sich die Beziehung: I0 ≈ c(x) * m(x) [6] Mit Einf³hrung einer Proportionalitõtskonstanten a(x) ergibt sich dann f³r das Na+-Ion der Stromstõrken-Anteil: I(Na+) = a * m(Na+) * c(Na+) [7] Zu Beginn der Reaktion gilt dann f³r beide Ionen: I0 = (a * m(Na+) * c0(Na+)) + (a * m(OH¢) * c0(OH¢)) [8] Bezeichnet man die OH¢-Konzentration zum Zeitpunkt t = 0 mit c0, so gilt aus Gr³nden der Elektroneutralitõt: c0(OH¢) = c0(Na+) = c0 [9] Daraus folgt f³r die Stromstõrke zum Zeitpunkt t = 0: [9] in [8]: I0 = (a * m(Na+) * c0) + (a * m(OH¢) * c0)) [10] bzw. zusammengefasst: |
||||||||
|
||||||||
|
b) Reaktionsphase
I = (a * m(Na+) * c(Na+)) + (a * m(OH¢) * c(OH¢)) +(a * m(Ac¢) * c(Ac¢)) [13] Die Na+-Ionenkonzentration bleibt wõhrend der ganzen Reaktion konstant: c(Na+) = c0(Na+) = c0 [14] Im Gegensatz dazu õndert sich die OH¢-Ionenkonzentration, da das Hydroxid-Ion in die Reaktion eingeht. Daher soll c(OH¢) = c sein. [15] Aufgrund der Elektroneutralitõt gilt: c(OH¢) + c(Ac¢) = c(Na+) [16] Die Summe der negativen Ladungen muss gleich sein der Summe der positiven Ladungen: [14] und 15] in [16]: c + c(Ac¢) = c0 [17] Daraus ergibt sich f³r die Ac¢-Konzentration der Term: c(Ac¢) = c0 - c [18] Wenn in Term [13] I = (a * m(Na+) * c(Na+)) + (a * m(OH¢) * c(OH¢)) + (a * m(Ac¢) * c(Ac¢)) [13] mit c(Na+) = c0 [14], c(Ac¢) = c0 - c [18] und c(OH¢) = c [15] folgende Substitutionen durchgef³hrt werden, ergibt sich der Ausdruck f³r die Stromstõrke zum Zeitpunkt t: I = (a * m(Na+) * c0) + (a * m(OH¢) * c) + (a * m(Ac¢) * (c0 - c)) [19] bzw. I = (a * m(Na+) * c0) + (a * m(OH¢) * c) + (a * m(Ac¢) * c0) - (a * m(Ac¢) * c) [20] Zusammengefasst:
|
||||||||
|
c) Endphase:
die Reaktion ist beendet. Am Ende der Reaktion bei t = ∞
liegen nur noch die Ac¢- und die Na+-Ionen
in gleicher Konzentration c0 vor, da die OH¢-Ionen ja verbraucht wurden: I∞ = I(Na+) + I(Ac¢) [22] = (a * m(Na+) * c(Na+)) + (a * m(Ac¢) * c(Ac¢)) [23] Mit c(Na+) = c0 [14] und c(Ac¢) = c0 - c [18] ergibt sich daraus: I∞ = (a * m(Na+) * c0) + (a * m(Ac¢) * (c0 - c)) [24] und da c = c(OH¢) [15] am Ende der Reaktion den Wert 0 erreicht hat, gilt: I∞ = (a * m(Na+) * c0) + (a * m(Ac¢) * c0) [25] Somit gilt f³r die Stromstõrke zur Zeit t = ∞ |
||||||||
|
||||||||
| Graphische Darstellung der verschiedenen Gr÷▀en: | ||||||||
 |
||||||||
| Um aus den gemessenen
Stromstõrken I0, I und I∞ die
gesuchte
Konzentration c zu erhalten, m³ssen die ³brigen Unbekannten (a, m(Na+),
m(Ac¢) und m(OH¢) entweder experimentell bestimmt
oder durch passende mathematische
Operationen eliminiert werden.
m(Na+) lõsst sich sehr einfach eliminieren, wenn man Stromstõrkedifferenzen bildet: I0 - I∞ = (a * c0 * (m(Na+) + m(OH¢))) - (a * c0 * (m(Na+) + m(Ac¢))) [27] = (a * c0 * m(Na+)) + (a * c0 * (m(OH¢)) - (a * c0 * m(Na+)) - (a * c0 * (m(Ac¢)) [28]
F³r die zweite Differenz gilt:
= (a * c0
* (m(Na+)) + (a * c0 * m(Ac¢)) + (a * c
* (m(OH¢)) - (a * c * m(Ac¢)) - (a * c0
* = (a * c * m(OH¢)) - (a * c * m(Ac¢)) [32]
Zwischenergebnis:
|
||||||||
|
(I0
- I∞)
= a * c0 *
(m(OH¢) - a * c0
* m(Ac¢) (I - I∞) a * c * (m(OH¢) - a * c * m(Ac¢) [34]
= a *
(m(OH¢) - a * m(Ac¢)
* c0 (I0
- I∞)
= c0 Dann ist
Da die Stromstõrke der Leitfõhigkeit proportional ist, gilt diese Gleichung auch f³r die Leitfõhigkeit:
|
||||||||
|
4.
Anwendung:
siehe Arbeitsblatt äReaktionen 2. Ordnung" 5. Auswertung: siehe Text äAuswertung des Versuchs zur alkalischen Esterhydrolyse" |
||||||||
Literatur: Tausch/v. Wachtendock: Chemie SII; Stoff - Formel - Umwelt; C.C. Buchner-Verlag. Bamberg 1993 Lutz Strohmaier: Chemie Sekundarstufe II, Verlauf chemischer Reaktionen; Schwann Verlag D³sseldorf 1978 |
||||||||
|
|