|
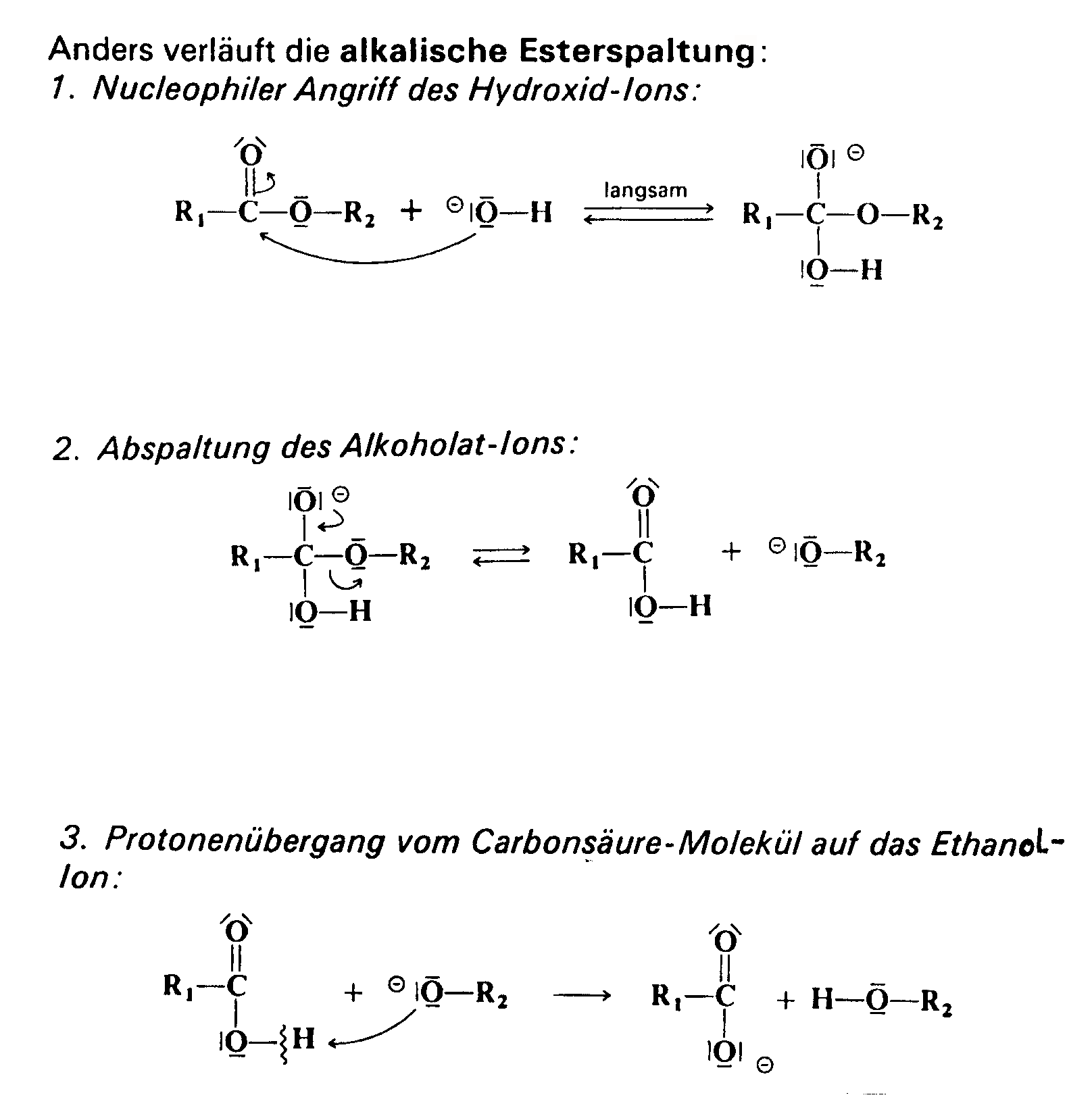
Mechanismus der Ester-Hydrolyse |
||||
siehe dazu: Reaktionen 2. Ordnung Die säurekatalysierte Esterhydrolyse führt immer zu einem Gleichgewicht. Die alkalische Esterhydrolyse spaltet dagegen Ester quantitativ. Die alkalische Esterhydrolyse heißt auch Verseifungsreaktion, weil diese Reaktion bei der Seifenherstellung verwendet wird.
|
||||
|
||||