| Alkane
(Paraffine, gesättigte KW,
Grenzkohlenwasserstoffe) bilden unverzweigte Ketten aus C-Atomen,
verzweigte Ketten oder ringförmige Moleküle (Cycloalkane).
Allein ihre Vielfalt bedingt eine Systematik der Benennung, die
überall auf der Welt einheitlich und verständlich ist: die sog.
Nomenklatur
der
International
Union of
Pure and
Applied
Chemistry (IUPAC).
Die anderen
Benennungen
der Alkane geben einen Hinweis
auf ihre chemischen Eigenschaften:
„Grenzkohlenwasserstoffe,"
weil die Grenze der Sättigung mit Wasserstoff erreicht ist;
Paraffine
(parum affinum = geringe Verwandtschaft) deutet auf eine
geringe Reaktionsbereitschaft hin
Die
gasförmigen Alkane C1 bis C4
reagieren in Gemischen
mit Luft/Sauerstoff unterschiedlicher Zusammensetzung durchaus
explosiv, z.B. Erdgas = Methangas. Von
C6 - C8 (Benzin und
seinen verwandten Verbindungen) ist bekannt, dass sie mehr oder
weniger leichtentzündlich sind und explosiv mit Luft/Sauerstoff
reagieren können. Kerzenwachs
(C14 - C16) ist in
flüssiger Form brennbar. Wie kommt es dann, dass sie durch
Säuren wie Salz-, Schwefel- oder Salpetersäure nicht angegriffen
werden? Warum reagieren sie nicht mit starken Laugen wie Natron-
oder Kalilauge? |
| Name |
Strukturformel |
Summenformel |
| Methan |
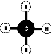 |
CH4 |
| Ethan |
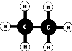 |
C2H6 |
| Propan |
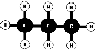 |
C3H8 |
| Butan |
|
|
| Pentan |
|
|
| Hexan |
|
|
| Heptan |
|
|
| Octan |
|
|
| Nonan |
|
|
| Decan |
|
|
|