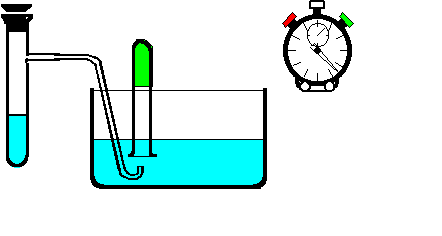
Stärke einer Säure bzw. Base (I)Praktikumsversuch I:Folgende Chemikalien werden abgewogen bzw. abgemessen: |
||||||||||||||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||||||||||||||
| Geräte:
Waage, Messzylinder,
Pipetten, Messkolben, PE-Flaschen mit aqua dest., pH-Meter; Durchführung: Stelle im Messkolben jeweils exakt 1 Liter Lösung aus den oben angegebenen Verbindungen her. Das Verfahren wird mündlich erläutert. Gib dann jeweils ca. 50 mL Lösung in ein kleines Becherglas und messe den pH-Wert mit dem vorher geeichten pH-Meter. Verdünne dann jede der 6 Lösungen auf das Zehnfache (wie geht das?) und messe erneut den pH-Wert. Trage alle Messwerte in die Tabelle ein. Messwert-Tabelle: |
||||||||||||||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||||||||||||||
|
Aufgaben:
1. Berechne die Stoffmengenkonzentration der Verbindungen a) bis f) in den Lösungen. (n=m/M; c=n/V) a) ___________ b)____________ c)____________ d)____________
e)_____________ f)____________ . 4. Ordne die untersuchten Säuren und Basen nach Stärke: Trage hier nur Vorschläge ein! Säuren: _________________________________________________________________________ Basen: _________________________________________________________________________ |
|
|
| Es empfiehlt sich, die dort angegebenen Volumina von Salzsäure, Essigsäure und Ammoniak in Verbindung mit der Dichte und dem Volumengehalt auf die in der Sammlung konkret vorhandenen Chemikalien abzustimmen, da sonst die Stoffmengenkonzentration nicht in allen sauren und alkalischen Lösungen gleich 0,2 mol/L beträgt. Entsprechend dem didaktischen Ansatz ist die Gleichheit der Konzentrationen der Lösungen jedoch die conditio sine qua non, um auf die Säure- und Basendissoziationskonstante hin zu führen. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
zu Praktikumsversuch I: Aufgabe 1: 1. Berechne die Stoffmengenkonzentration der Verbindungen a) bis f) in den Lösungen. (n=m/M; c=n/V) Aus den Molaren Massen der beteiligten Elemente werden die Molaren Massen der Verbindungen berechnet (Summe der Molaren Massen der Atome). Dichte bzw. Massenanteile der vorgelegten sauren oder basischen Lösungen sind ebenfalls gegeben bzw. auf den entsprechenden Flaschenetiketten aufgedruckt. Vorgegebene Gleichungen: r
=
m/V [g/mL]; Massenanteil w(%) = m/mLsg *1/100 [g/g]
Aus den Molaren Massen der beteiligten Elemente werden die Molaren Massen der Verbindungen berechnet (Summe der Molaren Massen der Atome). Dichte bzw. Massenanteile der vorgelegten sauren oder basischen Lösungen sind ebenfalls gegeben bzw. auf den entsprechenden Flaschenetiketten aufgedruckt. Vorgegebene Gleichungen: r
=
m/V [g/mL]; Massenanteil w(%) = m/mLsg *1/100 [g/g] Ergebnis: a) - f): Die Lösungen haben die Stoffmengenkonzentration c(X) = 0,2 mol/L |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Aufgabe 2: Berechne aus den
gemessenen pH-Werten jeweils die H+-Ionenkonzentration
c(H3O+) und fülle die beiden letzten Spalten der
Tabelle aus. (Ergebnisse eines Lehrerversuchs)
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Aufgabe 3: Formuliere das
Reaktionsschema, das für alle Reaktionen der
untersuchten Säuren mit Magnesium gültig ist. 2 H3O+(aq) + Mg(s) ----> Mg2+(aq) + H2(g) + 2 H2O(l) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
update am: 02.02.21 zurück zur Hauptseite |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||