| 1. |
Für einen Versuch benötigt man hoch reines
Kupfer(II)-chlorid. Würden Sie diese Substanz mit einem Silber- oder
einem Nickel-Löffel aus der Vorratsflasche entnehmen? |
| 2. |
Entscheiden Sie anhand der Redoxreihe, in welche Richtung
die folgenden Reaktionen verlaufen:
Sn(s) + Ni2+(aq)
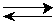 Sn2+(aq)
+ Ni(s)
Sn2+(aq)
+ Ni(s) |
Pb(s) + Sn2+(aq)
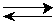 Pb2+(aq)
+ Sn(s) Pb2+(aq)
+ Sn(s) |
Ni(s) + Pb2+(aq)
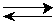 Ni2+(aq)
+ Pb(s)
Ni2+(aq)
+ Pb(s) |
Cu(s) + Hg2+(aq)
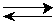 Cu2+(aq) + Hg(l)
Cu2+(aq) + Hg(l) |
|
| 3. |
Mit welchem Experiment könnte man zeigen, an welcher
Stelle Gold in die Redoxreihe einzuordnen ist? |
| 4. |
Beim Betrieb eines Daniell-Elementes nimmt die Masse der
Kupfer-Elektrode um 63,5 mg zu. Welche Ladungsmenge ist von der
Zink-Elektrode zur Kupfer-Elektrode geflossen? Um wie viel hat die Masse
der Zink-Elektrode abgenommen? |
| 5. |
Überlegen Sie, wie man a) die Stromstärke und b) die
Spannung in einer galvanische Zelle erhöhen kann. |
| 6. |
Wie kann die Spannung und der Stromfluss in der
"Zitronenbatterie" erklärt werden? |
| 7. |
Definiere folgende Begriffe:
a) Halbzelle, Halbelement, Halbkette;
b) Galvanisches Element
c) Daniell-Element
d) Potentialdifferenz
e) korrespondierendes Redoxpaar
f) Diaphragma
g) Anode, Kathode
h) Reihenschaltung, Parallelschaltung
i) elektrochemische Doppelschicht, Helmholtz-Doppelschicht;
j) Lösungstension
k) Sublimation
l) Hydratation
m) Ionisation
n) Redoxreihe
o) Standard-Elektrodenpotential
p) Normalpotential
q) Standard-Wasserstoff-Elektrode
r) platiniertes Platin
s) inerte Elektrode
t) Spannungsreihe
u) elektrische Arbeit |
|
|