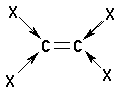Strukturdiagramm für die elektrophile AdditionIm Reaktionsmechanismus der Elektrophilen Addition gibt es verschiedene Faktoren, die auf einander wirken und den Mechanismus beeinflussen. In der folgenden Tabelle sind diese Faktoren aufgelistet:
Arbeitsauftrag: Bringe diese verschiedenen Faktoren detailliert und - wenn möglich - noch genauer aufgeschlüsselt in ein Strukturdiagramm, das die gegenseitigen Abhängigkeiten und Wechselwirkungen illustriert! Lösungsschritte 1. Zunächst müssen die einzelnen Faktoren weiter differenziert werden:
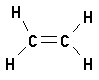
a) Struktur des Substrats:
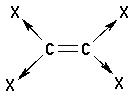
-I-Substituenten verringern die Elektronendichte
der C=C-Doppelbindung und damit deren Reaktivität.
b) Struktur des Agens:
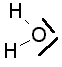
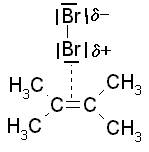
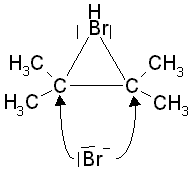
c) Einfluss und Struktur des Lösungsmittels: Vor allem für die unpolaren Agentien nach dem Schema X-X, die bei der elektrophilen Addition ja heterolytisch getrennt werden müssen, braucht es die Unterstützung des Lösungsmittels, das aufgrund seiner Struktur (v.a. Polarität) ionische oder zumindest Partialladungen stabilisieren kann. Je polarer das Lösungsmittel, desto besser die Unterstützung bei der heterolytischen Bindungstrennung von X-X-Molekülen. Damit wird aber das Lösungsmittel selbst zum Konkurrenten des eigentlichen Agens und reagiert als polares Molekül u.U. leichter mit dem Alken als das eigentliche Agens. Besitzt das Lösungsmittel polar gebundene H-Atome, reagiert es nach einem etwas anderen Mechanismus mit dem Substrat. d) Reaktionsmechanismus: In
jedem Fall verläuft die elektrophile Addition als zweischrittiger Prozess: im
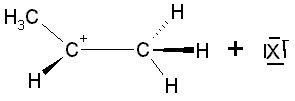
ersten langsamen und deswegen geschwindigkeitsbestimmenden Schritt wird b) Ähnlich verläuft die Addition eines Protons an die C=C-Doppelbindung, wenn Alkene mit H-haltigen Agentien oder Lösungsmitteln reagieren: der Spaltung der polarisierten Bindung H-X folgt die Addition des Protons an ein C-Atom und die Bildung des Carbenium-Ions am benachbarten C-Atom. Dabei ist es aber nicht möglich, einen cyclischen Übergangszustand zu bilden, da Wasserstoff als Element der ersten Periode maximal zwei Elektronen aufnehmen kann. Als Besonderheit dieses Schritts ist zu vermerken, dass das Proton von H-X an dem C-Atom addiert wird, das bereits H-Atome gebunden hat. Die Regel von Markownikow formuliert dies: "Denn der hat, dem wird gegeben werden." Hintergrund dieser Regel ist natürlich nicht die "biblische" Begründung, sondern die mögliche Entstehung von Methylgruppen, die mit ihrem +I-Effekt das Carbenium-Ion stabilisieren: Je mehr Methylgruppen entstehen, desto geringer ist der Energieaufwand zur Bildung dieses Schritts, weil die entstehende positive Ladung durch den +I-Effekt stabilisiert wird. c) In beiden Fällen ist nach der Ausbildung des Carbenium-Ions der nächste, schnelle und damit nicht geschwindigkeitsbestimmende Schritt die Addition eines Anions oder eines Nucleophils an das Carbenium-Ion. Diese Reaktion ist deswegen schnell, weil sie wie eine klassische Ionenreaktion erfolgt. Dabei bildet sich u.U. wieder ein geladenes Teilchen, das sich z.B. durch Protonenabspaltung stabilisiert.
Der Ein-Schritt-Mechanismus der elektrophilen Addition von Brom an Ethen in der Gasphase wird hier ausgeklammert! e). Strukturdiagramm |
| update am: 02.02.21 zurück zur Hauptseite |