Übungen
zur Nucleophilen Substitution
|
|
|
I. Formuliere die
Strukturformeln der folgenden Verbindungen in jeder
Gruppe und ordne die Verbindungen nach ihrer Reaktivität bei
SN2-Reaktionen:
a) 2-Brom-2-methylbutan, 1-Brompentan, 2-Brompentan
b) 1-Brom-3-methylbutan, 2-Brom-2-methylbutan, 2-Brom-3-methylbutan
c) 1-Brombutan, 1-Brom-2,2-dimethylpropan, 1-Brom-2-methylbutan,
1-Brom-3-methylbutan.
|
II. Stelle eine Reaktivitätsreihe für die Verbindungen jeder Gruppe bei
SN1-Reaktionen auf:
a) 2-Brom-2-methylbutan, 1-Brompentan,
2-Brompentan
b) 1-Brom-3-methylbutan, 2-Brom-2-methylbutan,
2-Brom-3-methylbutan
c) 1-Brombutan, 1-Brom-2,2-dimethylpropan,
1-Brom-2-methylbutan, 1-Brom-3-methylbutan.
|
III. Nimm als Beispiel ein beliebiges Alkylhalogenid und
NaOH in
wässriger Lösung. Vergleiche beide Mechanismen, indem Du eine Tabelle
mit einer Spalte für die SN1- und einer anderen für die
SN2-Reaktion
anfertigst, hinsichtlich folgender Kategorien:
a) der Stereochemie
b) der Reaktionsordnung
c) der relativen
Geschwindigkeit von CH3X,
C2H5X,
iso-C3H7X
und tert.-C4H9X.
d) der relativen Geschwindigkeit von R-Cl, R-Br und R-I.
e) des
Einflusses einer Verdoppelung der Konzentration von R-X auf die
Reaktionsgeschwindigkeit
f) des Einflusses
einer Verdoppelung der Konzentration von OH-
auf die Reaktionsgeschwindigkeit
g) des Einflusses der
Erhöhung des Wassergehaltes der Lösung auf die Reaktionsgeschwindigkeit
|
|
|
|
Lösungen |
I.
Formuliere die Strukturformeln der folgenden
Verbindungen in jeder Gruppe und ordne die Verbindungen nach ihrer
Reaktivität
bei SN2-Reaktionen: |
|
a) 2-Brom-2-methylbutan, 1-Brompentan,
2-Brompentan |
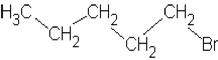 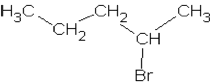
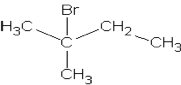 |
Die Reaktivität nimmt
für SN2-Reaktionen ab: zunehmende sterische Hinderung
erschwert SN2.
Die Reaktivität nimmt für SN1-Reaktion zu:
zunehmende Stabilisierung durch den +I-Effekt der Methylgruppen.
Sterische Hinderung und +-I-Effekt ergänzen sich und begünstigen SN1.
Unterschiede in der
RG bei SN2-Reaktionen sind hauptsächlich auf sterische Faktoren
und nicht auf elektronische Faktoren zurückzuführen.
Je größer die Anzahl
der Substituenten an dem Kohlenstoff ist, der das Halogen trägt, desto
kleiner wird die Reaktivität gegenüber einer SN2-Reaktion.
Unterschiede in der
RG bei SN1-Reaktionen sind hauptsächlich auf elektronische Faktoren
und nicht auf sterische Faktoren zurückzuführen.
|
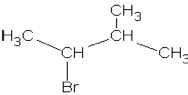
b)
1-Brom-3-methylbutan, 2-Brom-2-methylbutan,
2-Brom-3-methylbutan
SN2-Reihenfolge: |
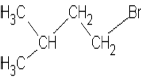
 |
|
Reaktivität für SN2 nimmt ab und für SN1 zu |
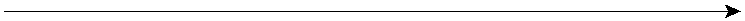 |
zunehmende sterische Hinderung erschwert SN2
zunehmender +I-Effekt begünstigt SN1
|
|
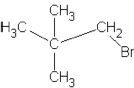
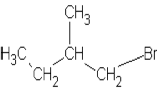
c) 1-Brombutan, 1-Brom-2,2-dimethylpropan,
1-Brom-2-methylbutan, 1-Brom-3-methylbutan. |

 |
 |
|
abnehmende sterische Hinderung durch die
Methyl-Gruppen begünstigt SN2;
abnehmende +I-Effekt erschwert SN1: der +I-Effekt ist aber nicht
stark vorhanden: das Reaktionszentrum ist immer ein primäres C-Atom.
|
III. Nimm als Beispiel ein beliebiges
Alkylhalogenid und NaOH in wässriger Lösung.
Vergleiche beide Mechanismen, indem Du eine
Tabelle mit einer Spalte für
die SN1- und einer anderen für die SN2-Reaktion
anfertigst, hinsichtlich folgender Kategorien:
| a) der Stereochemie |
| b) der Reaktionsordnung |
|
c) der relativen Geschwindigkeit von CH3X, C2H5X,
iso-C3H7X und tert.-C4H9X. |
| d) der relativen Geschwindigkeit von R-Cl, R-Br und
R-I. |
| e) des Einflusses einer Verdoppelung der
Konzentration von R-X auf die Reaktionsgeschwindigkeit |
|
f) des Einflusses einer Verdoppelung der
Konzentration von OH--Ionen auf die
Reaktionsgeschwindigkeit |
| g) des Einflusses der Erhöhung des Wassergehaltes
der Lösung auf die Reaktionsgeschwindigkeit |
|
|
|
| Kriterien |
SN1 |
SN2 |
|
Stereochemie |
Inversion und Retention: Racemisierung |
vollständige Inversion: Waldensche Umkehr |
|
Reaktionsordnung |
Reaktion 1. Ordnung |
Reaktion 2. Ordnung |
|
relative Geschwindigkeit von : Alkylstruktur |
CH3X < C2H5X
< iso-C3H7X < tert.-C4H9X. |
CH3X > C2H5X
> iso-C3H7X > tert.-C4H9X. |
|
relative Geschwindigkeit: Abgangsgruppe |
R-Cl < R-Br < R-I
Reaktivität ----> zunehmend |
R-Cl < R-Br < R-I
Reaktivität ----> zunehmend |
|
RG <–> Verdoppelung von c(RY) |
Verdoppelung von c(R-X)
verdoppelt die RG |
Verdoppelung von c(R-X)
verdoppelt die RG |
|
RG <–> Verdoppelung von c(OH-) |
Verdoppelung von c(OH-)
spielt keine Rolle |
Verdoppelung von c(OH-)
verdoppelt die RG |
|
RG <–> Erhöhung des Wassergehalts |
Erhöhung des Wassergehalts
steigert die RG |
Erhöhung des Wassergehalts beeinflusst nicht
wesentlich die RG |
|
Quelle: Morrison/Boyd: Lehrbuch der Organischen Chemie,
Weinheim 1974, Kapitel 14
Siehe dazu
auch
Übungen
zur Nucleophilen Substitution im pdf-Format und
Übungen
zur Nucleophilen Substitution im WordPerfect-Format
update:
02.02.21
zurück
zur Hauptseite
|







