|
Da der
aromatische Ring eine relativ hohe Elektrodendichte aufweist, wird er
bevorzugt von einem Elektronenmangel- Teilchen (
Agens) angegriffen. Deswegen ist die typische Reaktion aromatischer
Verbindungen nicht die
, sondern die
. Unterstützt wird dieser Mechanismus wie bei der
Addition von Brom an Alkene durch Stoffe, die eine des
Brom-Moleküls einleiten.
Diese Stoffe, sog. LEWIS-Säuren, reagieren mit dem Agens, hier Brom. Aus Eisen und einem
Teil des Broms entsteht somit___________ . Die
verläuft in zwei Schritten: |
|
LEWIS-Säuren
sind
Moleküle oder Ionen mit unvollständig besetzter äußerer
Elektronenschale. Sie können gegenüber anderen
Reaktionspartnern als Elektronenpaar-Akzeptoren wirken,
in dem sie eine kovalente Bindung mit dem Reaktionspartner
ausbilden.
LEWIS-Basen sind dagegen Moleküle oder Ionen mit freien
Elektronenpaaren. Sie können gegenüber anderen
Reaktionspartnern als Elektronenpaar-Donatoren wirken,
dabei kommt ebenfalls eine kovalente Bindung zustande. Das
Neutralisationsprodukt aus LEWIS-Säure und -Base ist ein
LEWIS-Säure-Base-Komplex. |
|
|
Unterstützung
durch die LEWIS-Säure im 1. Schritt der
Substitution eine hohe
. Dieser 1. Schritt ist deswegen der
langsamste,
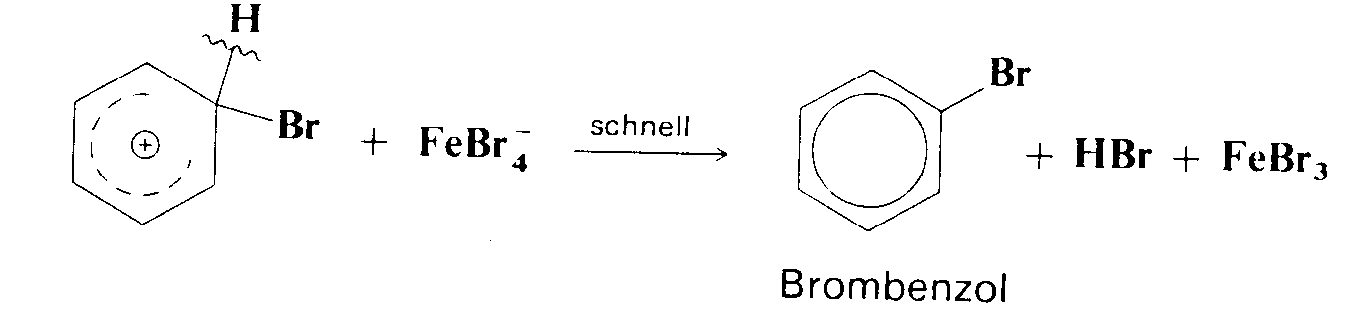
Schritt. Die Protonenabspaltung erfolgt dann als 2. Schritt
schnell, da der aromatische, nun substituierte Ring unter
Energie-Abgabe zurückgebildet wird. |
 |
|
Die Substitution ist also wegen der
gegenüber der Addition die bevorzugte Reaktion aromatischer
Systeme.
Quelle: Das Arbeitsblatt beruht auf den Ausführungen und Bildern von M. Tausch/M.v.Wachtendonk:
Chemie SII, Stoff-Formel-Umwelt", Bamberg 1993;
update am:
02.02.21
zurück
zur Hauptseite |