|
1. Bilde die Summe der Ionenradien f¸r die beiden Reihen
der Alkalihalogenide und der Erdalkalioxide und stelle den Zusammenhang zwischen
der Summe der Ionenradien und den Schmelzpunkten f¸r die beiden
Verbindungsgruppen graphisch dar (x-Achse: Summe der Ionenradien [in pm],
y-Achse: Schmelzpunkte [ ∞C]).
| Alkalihalogenide |
NaF |
NaCl |
NaBr |
NaI |
| Smp [∞C] |
993 |
801 |
747 |
660 |
| Ionenradien [pm] |
102 |
133 |
102 |
181 |
102 |
196 |
102 |
220 |
| Summe Ionenradien |
235 |
283 |
298 |
322 |
| Erdalkalioxide |
MgO |
CaO |
SrO |
BaO |
| Smp [∞C] |
2852 |
2927 |
2430 |
1918 |
| Ionenradien [pm] |
72 |
140 |
100 |
140 |
118 |
140 |
135 |
140 |
| Summe Ionenradien |
212 |
240 |
258 |
275 |

2. Vergleiche die beiden Gruppen: welcher Zusammenhang
zwischen Schmelzpunkt und Summe der Ionenradien ist zu vermuten? Definiere dazu
die zwei Gruppen: was sind die Gemeinsamkeiten, was sind die Unterschiede?
Bei beiden Gruppen wird deutlich, dass mit zunehmender
Summe der Ionenradien der Schmelzpunkt sinkt. Es besteht also eine
Proportionalit‰t zwischen der Summe der Ionenradien und dem Schmelzpunkt: Je
grˆfler die Summe der Ionenradien, desto niedriger der Schmelzpunkt. Das ist
nicht weiter verwunderlich, weil mit steigender Summe der Ionenradien auch die
Coulomb¥sche Anziehungskraft sinkt. Bei den Alkalihalogeniden ist der
Zusammenhang eindeutig, bei den Erdalkalioxiden "stˆrt" der Anstieg von MgO zu
CaO.
3. Wie lassen sich "Unregelm‰fligkeiten" oder "Ausnahmen"
erkennen?
Eine "Unregelm‰fligkeit" oder "Ausnahme" stellt der Anstieg
von MgO zu CaO dar, der dann folgende Abfall gehorcht wieder dem oben
beschriebenen Zusammenhang.
Die Ionen der Erdalkalimetalle sind
kleiner als die der Alkalimetalle und haben ein erheblich grˆfleres Verh‰ltnis
von Ionenladung zu Ionenradius. Eine der Konsequenzen dieser Erscheinung ist,
dass die Verbindungen des Berylliums und des Magnesiums einen nennenswert
kovalenten Anteil haben, also keinen reinen Ionenverbindungen sind, im Gegensatz
zu den darauf folgenden Metallverbindungen. Die erste "reine" Ionenverbindung
dieser Reihe ist also das Calciumoxid. Diese "Verschiebung" liegt letzten Endes
darin begr¸ndet, dass Beryllium und Magnesium zu den ersten drei Perioden im PSE
gehˆren und nach der 3. Periode die 4. mit den Nebengruppen beginnt (Elemente
Scandium bis Zink, 10 Elemente in 8 Nebengruppen). Einen ‰hnlichen Verlauf der
Eigenschaften kann man auch im
Datenblatt der Erdalkalimetalle erkennen.
4. Warum unterscheidet sich die Gruppe der Erdalkalioxide
so deutlich von der Gruppe der Alkalihalogenide?
Obwohl die Summe der Ionenradien der Erdalkalioxide
vergleichbar der der Alkalihalogenide ist, liegen die Schmelzpunkt fast dreifach
so hoch, auf jeden Fall wesentlich hˆher. Das kann nur darin begr¸ndet sein,
dass die Alkalihalogenide die Ladungszahl +1 bzw. -1 besitzen, die
Erdalkalioxide aber +2 bzw. -2 f¸r Sauerstoff. Die Ionen ziehen sich also mit
der doppelten Ladung an, was wesentlich hˆhere Coulomb¥sche Anziehungskr‰fte zur
Folge hat.
5. Erweitere die graphische ‹bung auf die
Kaliumhalogenide und die
Alkaliiodide: welche Aussagen lassen sich aus dem Vergleich
schlussfolgern?
| Kaliumhalogenide |
|
KCl |
KBr |
KI |
| Smp [∞C] |
770 |
734 |
681 |
| Ionenradien |
138 |
181 |
138 |
196 |
133 |
220 |
| Summe Ionenradien |
318 |
334 |
358 |
| Alkaliiodide |
NaI |
KI |
RbI |
|
| Smp [∞C] |
660 |
681 |
647 |
| Ionenradien |
102 |
220 |
138 |
220 |
148 |
220 |
| Summe Ionenradien |
322 |
358 |
372 |
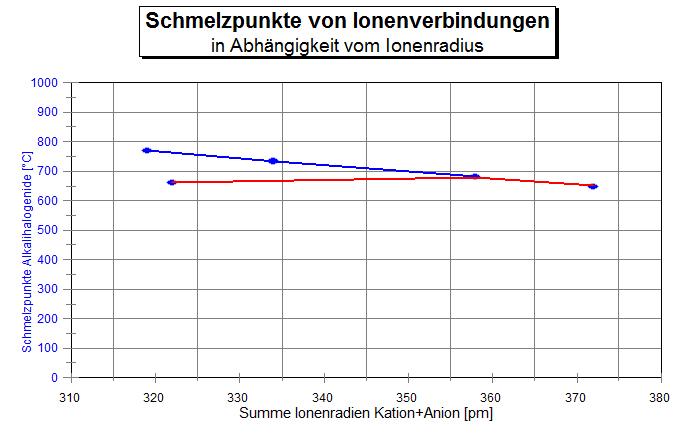
Kaliumhalogenide: Bei gleich bleibender Grˆfle des Kations und zunehmender Grˆfle des Anions steigt
die Summe der Ionenradien und der Schmelzpunkt sinkt. Der Zusammenhang
entspricht den oben angesprochenen Gesetzm‰fligkeiten.
Alkaliiodide:
Trotz steigender Summe der Ionenradien nimmt der Schmelzpunkt zu und f‰llt
erst ab KI wieder ab.
Der Grund d¸rfte in den "Verschiebungen"
der Eigenschaften (siehe Dichte im
Datenblatt Alkalimetalle) zu finden sein, die mit der
Erweiterung von der 3. Periode (Na) zur 4. Periode (K) verbunden sind. Das
"Ausnahmeelement" ist also Natrium. KI und RbI verhalten sich "regelgem‰fl".
|