|
Versuchsauswertung "Experimentelle Bestimmung von Massenverhältnissen" |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Zur Versuchsdurchführung: siehe das Arbeitsblatt
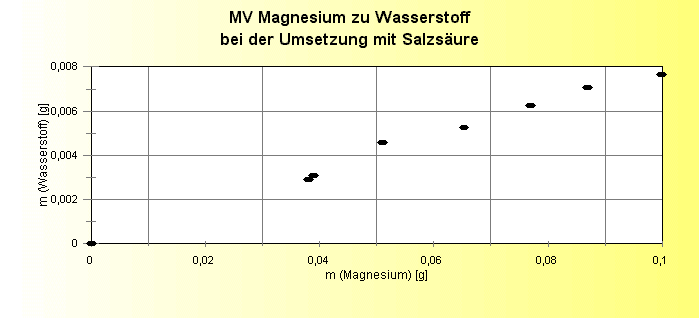
"In welchem Massenverhältnis verbinden sich Atome"? Reaktion von Magnesium mit Salzsäure Versuchsergebnisse:
Graphische Darstellung:
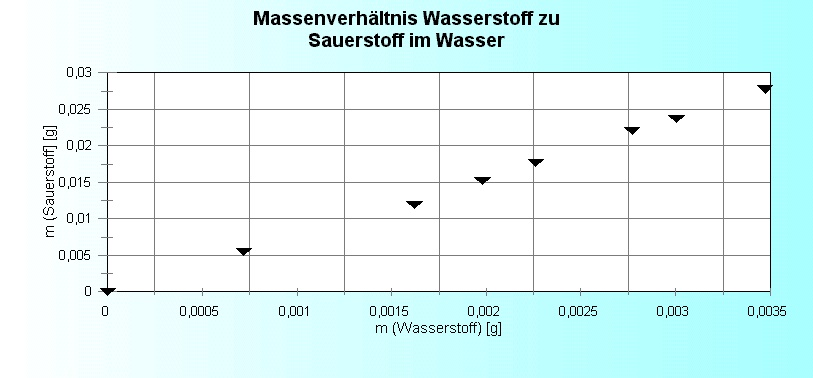
Elektrolyse von Wasser: Hoffmann-Wasserzersetzung
Graphische Darstellung:
Kommentar: Beide Versuche bestätigen nicht nur die Linearität des Massenverhältnisses von Magnesium zu Wasserstoff bzw. Wasserstoff zu Sauerstoff, sondern sind auch Grundlage dafür, auf die Atommassen von Magnesium und Sauerstoff zu schließen. Danach ist Magnesium 12,5 mal so schwer wie Wasserstoff und Sauerstoff 8 mal so schwer. In einem weiteren Schritt wird nun über die Verknüpfung der Volumenverhältnisse bei der Wasseranalyse und der 1:1-Zusammensetzung von Magnesiumoxid darauf geschlossen, dass jeweils 2 Teilchen Wasserstoff auf ein Teilchen Magnesium bzw. Sauerstoff kommen. Daraus ergibt sich dann erst das richtige Massenverhältnis von 1: 24,3 bzw. 1:16. |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
update: 01.02.21 zurück zur Hauptseite |