|
L÷sungen: |
||||||||||||||||||||||||||||||
|
1.
Beobachtungen zu den drei Versuchen:
V1a: Beide Fl³ssigkeiten mischen sich nicht, das spezifisch leichtere (kleinere Dichte) Pentan bildet die obere Phase, Wasser die untere. V1b: Beide Fl³ssigkeiten mischen sich und bilden eine gemeinsame Mischphase. V1c: Beide Fl³ssigkeiten mischen sich und bilden eine gemeinsame Mischphase. V2: Bei portionsweiser Zugabe von ca. 10 mL Ethanol verschwindet gegen Ende der Zugabe die Pentan-Phase.
V3:
Jod
l÷st sich gut in Pentan und in Ethanol, schlecht in Wasser.
Glucose
l÷st sich dagegen gut in Wasser, mõ▀ig l÷slich in Ethanol und schlecht
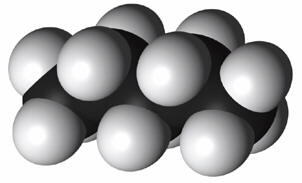
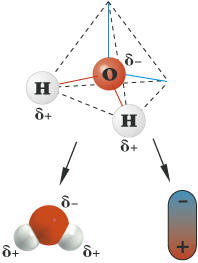
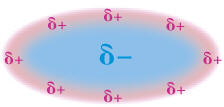
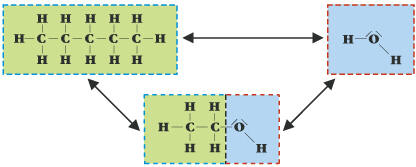
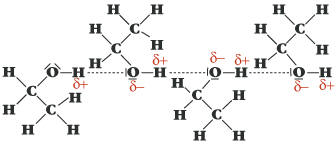
l÷slich in Pentan. Erklõrungen zu den Versuchen: Gemõ▀ dem Lehrsatz "Similia similibus solvuntur" (siehe Punkt e): "─hnliches wird von ─hnlichem gel÷st" weisen die Versuchsergebnisse auf strukturelle Gemeinsamkeiten und Unterschiede hin, die die L÷slichkeit bzw. Unl÷slichkeit erklõren. Pentan ist ein Kohlenwasserstoff, in diesem Falle nur aus 5 Kohlenstoff- und 12-H-Atomen zusammengesetzt (siehe Hinweis a). Die C-Atome bilden eine Kette, die H-Atome umh³llen diese, die Atome beider Elemente sind mit Elektronenpaarbindungen an einander gebunden. Zwischen beiden Elementen besteht nur ein geringer Unterschied in der Elektronegativitõt, der aufgrund der molekularen Symmetrie praktisch nicht zum Tragen kommt. Deswegen bilden Pentan-Molek³le untereinander auch nur schwach wirkende Van-der-Waals-Krõfte aus, also fluktuierende, temporõre schwache zwischenmolekulare Anziehungskrõfte, die von der Molek³lgr÷▀e (Oberflõche!) und dem Abstand sowie der Temperatur abhõngig sind. Wasser bildet mit Wasserstoff- und Sauerstoffatomen aufgrund des gro▀en Unterschiedes in der Elektronegativitõt und des Bindungswinkel ein stark polares Molek³l. Die Wassermolek³le werden zusammengehalten nicht nur durch ihre Dipoleigenschaft, sondern auch wesentlich durch die Ausbildung der Wasserstoffbr³ckenbindung, der stõrksten zwischenmolekularen Bindungsart bei den Sekundõrbindungen. Ethanol steht gewisserma▀en dazwischen: ohne all zuviel metaphorische Vergleiche anstrengen zu wollen, besitzt es Anteile des Pentans mit seiner aus zwei C-Atomen bestehenden Kohlenstoffkette, die von 5 H-Atomen umgeben ist und Anteile des Wassers in Form der Hydroxy-Gruppe, die als Abk÷mmling (Derivat) des Wassers betrachtet werden kann. Somit vereinigt Ethanol sowohl Eigenschaften des Pentans wie auch des Wassers in sich und ist somit das ideale Vermittlermolek³l zwischen niederen Kohlenwasserstoffen (C-Zahl bis ca.7) und Wasser, einem der polarsten Stoffe, die es gibt. Jod bildet im festen Zustand ein kristallines Gitter aus Jod-Atomen, das durch ebensolche Van-der-Waals-Bindungen zusammen gehalten wird. Das Gitter aus nur einer Art von Atomen eines Elements ist unpolar. Wegen der ─hnlichkeit der Bindungen l÷st sich Jod in Pentan hervorragend, ist Ethanol ganz gut (─hnlichkeit mit dem Kohlenwasserstoffanteil), in Wasser schlecht, weil die Sekundõrbindungsverhõltnisse v÷llig verschieden sind (Van-der-Waals-Bindungen versus Wasserstoffbr³ckenbindung). Das gleiche gilt f³r Glucose, die aufgrund der Struktur (Summenformel C6H12O6) f³nf Hydroxy-Gruppen aufweist, die somit sehr gute Bindungen zu Wasser eingehen k÷nnen, mõ▀ig gute Bindungen zu Ethanol, aber keine zu Pentan. Der Nebeneffekt der gemeinsamen Farbe in Wasser und Ethanol, unterschiedlich zu Pentan, weist ebenfalls auf strukturelle Gemeinsamkeiten von Wasser und Ethanol hin (s.o.: Ethanol als Derivat von Wasser).
Bild-Quelle: Tausch/v. Wachtendonk: Chemie 2000+ ▄brigens:
Tragendes Element f³r das Molek³lger³st des Pentans wie auch der
Alkohole ist der Kohlenstoff. Kohlenstoff wird mit dem Elementsymbol
C f³r Carbon im Periodensystem aufgef³hrt. Es hat die Ordnungszahl 6
und ist der 4. Hauptgruppe zugeordnet. In der Natur kommt Carbon in
gediegener als auch in chemisch-gebundener Form vor.
Carbon gilt als eines der wichtigsten Materialien f³r die Zukunft des Autobaus. Da die Kohlenstofffaser-Verbindungen halb so leicht wie herk÷mmliches Aluminium und hõrter als Stahl sind, soll der Treibstoffverbrauch der Autos somit gesenkt werden. Doch neben diesen n³tzlichen Eigenschaften hat Carbon f³r den Verbraucher einen ganz besonderen Nutzen: Carbon sieht hochwertig aus und steht f³r Sportlichkeit sowie Dynamik, da es im Rennsport weit verbreitet ist. Aufgrund dessen erfreuen sich Accessoires wie Schmuck aus Carbon, Carbon-Eheringe oder auch Uhren mit Carbon-Elementen gro▀er Beliebtheit.
update am: 02.02.21 zur³ck zur Hauptseite |