Bestimmung der Geschwindigkeitskonstanten der Alkalischen
Esterhydrolyse
Der Versuch wird nach der Anleitung im Arbeitsblatt
"Reaktionen
2. Ordnung" durchgeführt.
1. Messergebnisse der Leitfähigkeitsmessung mit der Chembox:
Die Anfangsleitfähigkeit c0 betrug
5,2 mS, die Endleitfähigkeit cende 2,0 mS
bei 22 °C nach 24 Stunden .
|
t [s] |
20 |
40 |
60 |
80 |
100 |
120 |
140 |
160 |
180 |
200 |
220 |
240 |
260 |
280 |
300 |
|
LF [mS] |
5,03 |
4,905 |
4,785 |
4,66 |
4,563 |
4,464 |
4,366 |
4,289 |
4,213 |
4,14 |
4,082 |
4,013 |
3,95 |
3,898 |
3,845 |
|
t [s] |
320 |
340 |
360 |
380 |
400 |
420 |
440 |
460 |
480 |
500 |
520 |
540 |
560 |
580 |
600 |
|
LF [mS] |
3,794 |
3,743 |
3,702 |
3,661 |
3,621 |
3,586 |
3,545 |
3,514 |
3,482 |
3,449 |
3,412 |
3,382 |
3,358 |
3,326 |
3,301 |
|
t [s] |
620 |
640 |
660 |
680 |
700 |
720 |
740 |
760 |
780 |
800 |
820 |
840 |
860 |
880 |
900 |
|
LF [mS] |
3,281 |
3,254 |
3,233 |
3,211 |
3,191 |
3,161 |
3,148 |
3,121 |
3,108 |
3,067 |
3,067 |
3,056 |
3,036 |
3,016 |
3,012 |
|
t [s] |
920 |
940 |
960 |
980 |
1000 |
1020 |
1040 |
1060 |
1080 |
1100 |
1120 |
1140 |
1160 |
1180 |
1200 |
|
LF [mS] |
2,994 |
2,979 |
2,957 |
2,949 |
2,938 |
2,923 |
2,911 |
2,894 |
2,884 |
2,869 |
2,863 |
2,854 |
2,843 |
2,827 |
2,824 |
2. Graphische Darstellung der Leitfähigkeits-Zeit-Kurve:

Wenn man mit einem Kurvenlineal arbeiten will, ist es besser,
die Linieneinstellung in den Bereichseigenschaften auf "keine" zu
stellen. Manche Programme verbinden die Messpunkte mit Geraden, andere mit
Kurvenstücken, die dem Verlauf besser angepasst sind.
3. "Arbeitsdiagramm" mit den grundlegenden
graphischen und geometrisch-proportionalen Beziehungen.
EEE: Essigsäureethylester
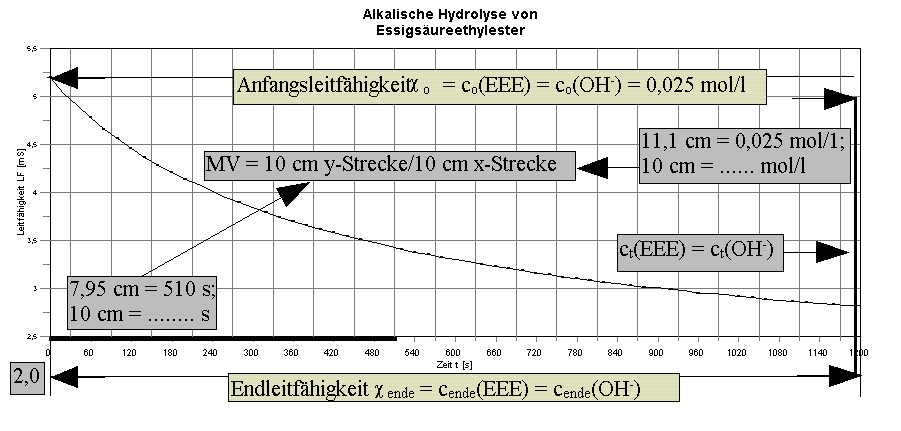
Je nach Größe des Ausdrucks (Hoch- oder Querformat,
Seitenränder usw.) bekommt man eine Graphik, bei der der
Anfangsleitfähigkeitswert bei t=0, c0 =
5,2 mS auf der linken y-Achse mit dem entsprechenden Punkt auf der rechten
y-Achse parallel zur Zeit-Achse verbunden wird. Dadurch erhält man den Punkt c0(EEE)
= c0(OH-) = 0,025 mol/l.
Analog verfährt man mit dem Endpunkt der Leitfähigkeit cende
= eende(EEE) = eende(OH-) . Da der Endpunkt 2,0
auf der linken y-Achse nicht drauf ist, erstellt man ihn entweder durch
entsprechende Einstellungen der Achsenskalierung im Computer-Programm oder per
Hand, indem man entsprechende Größenabschnitte nach unten verlängert. Die
angegebenen Zahlen sind Beispiele aus einem real existierenden Ausdruck.
4. Werte-Tabelle für die Ermittlung des
Zeitgesetzes:
|
Auswertung von Graph_I |
|
alpha-Werte |
a1 |
a2 |
a3 |
a4 |
a5 |
a6 |
a7 |
a8 |
|
Wert |
53,7 |
44,5 |
33,4 |
27,5 |
20,5 |
16 |
10,7 |
6,5 |
|
tan a |
1,3613 |
0,9827 |
0,6594 |
0,5206 |
0,3739 |
0,2867 |
0,1890 |
0,1139 |
|
RG=tan a
* MV |
4,973E-05 |
3,590E-05 |
2,409E-05 |
1,902E-05 |
1,366E-05 |
1,048E-05 |
6,903E-06 |
4,162E-06 |
|
Abstand von cende(OH)‾ [cm] |
11,7 |
10,05 |
8,45 |
7,2 |
6,2 |
5,45 |
4,6 |
3,75 |
|
ct(OH‾ ) [mol/l] |
2,224E-02 |
1,911E-02 |
1,606E-02 |
1,369E-02 |
1,179E-02 |
1,036E-02 |
8,745E-03 |
7,129E-03 |
|
|
|
Daten für die Graphik |
|
ct(OH‾ ) [mol/l] |
2,22E-02 |
1,91E-02 |
1,61E-02 |
1,37E-02 |
1,18E-02 |
1,04E-02 |
8,75E-03 |
7,13E-03 |
|
(ct(OH‾ )2 [mol/l]2 |
4,95E-04 |
3,65E-04 |
2,58E-04 |
1,87E-04 |
1,39E-04 |
1,07E-04 |
7,65E-05 |
5,08E-05 |
|
RG=tan
a * MV |
4,97E-05 |
3,59E-05 |
2,41E-05 |
1,90E-05 |
1,37E-05 |
1,05E-05 |
6,90E-06 |
4,16E-06 |
Maßstabsverhältnis: 3,653*10-5
5. Graphische Darstellung der Zeitgesetze:
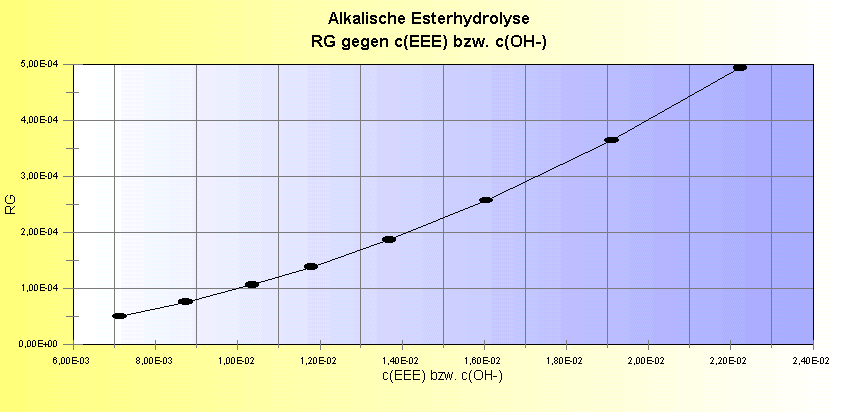
beziehungsweise:
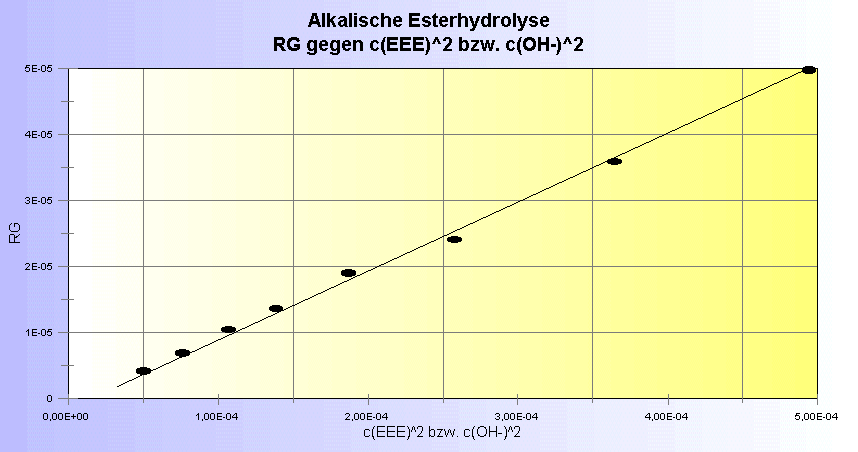
Die Steigung der Geraden betrug a = 26°, damit
erhielt k den Wert von: k = 0,1026 L/mol*s
Zur Auswertung des Leitfähigkeits-Zeit-Graphen und zur
Erstellung der Graphiken für die Geschwindigkeitsbeziehung siehe auch "Anleitung zu Auswertung des Versuchs zur
Alkalischen Esterhydrolyse". |



