Versuchsergebnisse zur Reaktion von Natriumthiosulfat mit Salzs‰ure
|
Versuchsergebnisse |
|
|
|
Rechnerische Umsetzung der Versuchsergebnisse in graphisch
verwertbare Daten |
|
Gruppe |
1 |
2 |
3 |
4 |
|
5 |
6 |
|
7 |
8 |
|
Tobias v.Sp.
Valerie K.
Cem K. |
Andre' F.
Thomas Z.
Tobias S. |
Thomas Zi.
Oliver H. |
Dennis S.
Chantal E. |
MW von
1-4 |
Melanie W.
Vanessa S.
Christian K. |
Malika B.
Jasmine T.
Cornelia L. |
MW von
5&6 |
Andre' H.
Rene L.
Raph‰l S. |
Thomas K.
Alexander H. |
|
V-Nr. |
|
1 |
138 |
140 |
133 |
140 |
137,75 |
60 |
55 |
57,5 |
46 |
64 |
|
2 |
273 |
313 |
230 |
250 |
266,5 |
135 |
105 |
120 |
68 |
262 |
|
3 |
414 |
473 |
400 |
360 |
411,75 |
235 |
162 |
198,5 |
75 |
297 |
|
4 |
573 |
650 |
510 |
480 |
553,25 |
330 |
251 |
290,5 |
126 |
312 |
|
5 |
703 |
702 |
720 |
678 |
700,75 |
440 |
291 |
365,5 |
204 |
390 |
|
tR |
21 |
21 |
21 |
21 |
|
30 |
30 |
|
40 |
? |
Die Werte aus Gruppe 8 sind nicht auswertbar, da die
Temperatureinstellung der Lˆsungen nicht genau genug erfolgte.
|
1. Schritt:
Berechnung der Thiosulfat-Konzentration
c(Thio) und Salzs‰ure-Konzentration c(HCl) aus den Versuchsangaben. Der Rechengang folgt der
Methode, die auf der Seite
"Konzentrationen"
erl‰utert wird. Die Zeiten f¸r die Gesamtreaktionsdauer sind die aus
den 4 Versuchsgruppen gemittelten Zeiten. |
Tabelle 1:
Ergebnisse des im 1. Schritt dargelegten Rechengangs.
|
|
MW |
MW |
|
|
R.-dauer |
R.-dauer |
R.-dauer |
|
V-Nr. |
V(Thios.) |
V(Wasser) |
V(HCl) |
c(Thios.) |
c(HCl) |
t=21 ∞C |
t=30 ∞C |
t=40 ∞C |
|
1 |
50 |
0 |
5 |
0,045455 |
0,181818 |
138 |
58 |
30 |
|
2 |
50 |
50 |
5 |
0,023810 |
0,095238 |
267 |
120 |
45 |
|
3 |
50 |
100 |
5 |
0,016129 |
0,064516 |
412 |
199 |
75 |
|
4 |
50 |
150 |
5 |
0,012195 |
0,048780 |
553 |
291 |
126 |
|
5 |
50 |
200 |
5 |
0,009804 |
0,039216 |
701 |
366 |
204 |
Die graphische Umsetzung zeigt die Zunahme der Reaktionsdauer
mit abnehmender Konzentration der beiden Reaktionsteilnehmer. Die Graphik stellt
nur die Versuchsergebnisse bei t=21 ∞C dar.

Die
graphische Auswertung
und Berechnung der Konzentrationen
gibt aber keine Antwort auf die Frage, ob die Konzentrationen beider
Reaktionspartner oder nur die eines (und wenn ja: welcher)
die Reaktionsdauer bestimmen.
Mit der
Methode der Numerischen Differentation
bestimmt man
Konzentrationsdifferenzen, die auf Zeitdifferenzen bezogen werden. Damit hat man
die Reaktionsgeschwindigkeit als Quotient aus Konzentrations- und Zeitdifferenz
gebildet.
|
2. Schritt:
Aus der
Subtraktion c1(Thio) -
c2(Thio) ergeben sich die Δc(Thio)-Werte. Dieselbe Methode wird verwendet bei der Bestimmung von
Δc(HCl)
und Δt. Aus den Δc(Thio)- und Δc(HCl)-Werten
wird durch Division mit Δt der entsprechende Wert
Δc(Thio)/Δt
bzw. Δc(HCl)/Δt.
Damit sind die entsprechenden
Reaktionsgeschwindigkeitswerte numerisch gebildet. Die Daten gelten nur
f¸r die Reaktionstemperatur von 21 ∞C.
|
Tabelle 2: Ergebnisse des 2. Rechenschritts
|
|
MW
R.-dauer
t=21 ∞C |
|
|
|
dc(Thio)
dt
|
dc(HCl)
dt
|
|
|
c(Thios.) |
c(HCl) |
dc(Thio) |
dc(HCl) |
dt |
|
V-Nr. |
[mol/L |
[mol/L] |
[mol/L] |
[mol/L] |
[s] |
[mol/Ls] |
[mol/L/s] |
|
1 |
0,0455 |
0,1818 |
138 |
|
|
|
|
|
|
2 |
0,0238 |
0,0952 |
267 |
0,0216 |
0,0866 |
128,8 |
1,68E-04 |
6,72E-04 |
| 3 |
0,0161 |
0,0645 |
412 |
0,0077 |
0,0307 |
145,3 |
5,29E-05 |
2,12E-04 |
|
4 |
0,0122 |
0,0488 |
553 |
0,0039 |
0,0157 |
141,5 |
2,78E-05 |
1,11E-04 |
|
5 |
0,0098 |
0,0392 |
701 |
0,0024 |
0,0096 |
147,5 |
1,62E-05 |
6,48E-05 |
|
3. Schritt: Aus den Konzentrationswerten c1(Thio) und c2(Thio) aus
den Versuchen 1 und 2
wird ein
Mittelwert gebildet. Dasselbe Verfahren wird mit
c2 und c3 usw. analog fortgesetzt und ebenso auf c1(HCl) und c2(HCl) ¸bertragen. Zur
Darstellung der Graphik werden die c(Thio)-Mittelwerte auf der x-Achse aufgetragen und die
dc(Thio)/dt-Werte auf der y-Achse. Dasselbe wird mit c(HCl)-Mittelwerte und dc(HCl)/dt
gemacht. |
Tabelle 3: Zusammengefasste Rechenergebnisse f¸r die
Graphik-Darstellung:
MW
c(Thio)
[mol/l] |
dc(Thio)
dt
[mol/l/s] |
MW
c(HCl)
[mol/l] |
dc(HCl)
dt
[mol/l/s] |
|
0,035 |
1,68E-04 |
0,139 |
6,72E-04 |
|
0,020 |
5,29E-05 |
0,080 |
2,12E-04 |
|
0,014 |
2,78E-05 |
0,057 |
1,11E-04 |
|
0,011 |
1,62E-05 |
0,044 |
6,48E-05 |
Ergebnisse der graphischen Umsetzung:
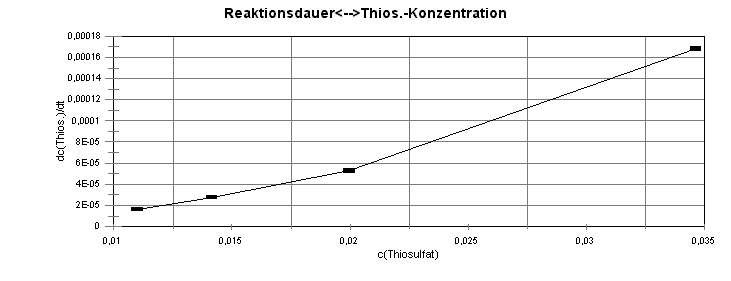

Beide Abbildungen zeigen eine
fast lineare Abh‰ngigkeit der
Reaktionsgeschwindigkeit von der Konzentration beider Teilnehmer. Damit kann
diese Reaktion auch zur Einf¸hrung des Begriffs der
Momentangeschwindigkeit
genommen werden und zur
graphischen Bestimmung der
Geschwindigkeits-Konstanten.
Aus didaktischen Gr¸nden wird aber die
Reaktion
Magnesium-Salzs‰ure dem vorgezogen, weil sie als Reaktion pseudo-1.-Ordnung
leichter und genauer auszuwerten ist. |


